不同行业由于积累的数据量庞大、数据种类多样、业务形态繁杂,以及拥有机构或个人机密信息,其数据价值和利益巨大,面对的潜在安全隐患更是无处不在。勒索病毒、人为损坏,或是由于不可控的意外灾害,都可能导致原始数据被篡改和丢失等严重情况,为此监管机构和行业协会出台相关规范、管理办法和行业标准,来规范企业对于数据的记录、存储和管理。

例如很多企业需遵循《数据安全法》、《网络安全法》、《个人信息保护法》等,对通过网络或以电子等形式进行收集、存储、传输、使用、提供、公开数据等环节进行规范,并规定了网络产品和服务者的义务。
而其中,医药行业与人类生命健康息息相关,受到卫健委、工信部、医保局、药监局等多方监管单位的监督和管理。以确保研发、生产、临床试验和临床医疗及用药等过程中的数据和信息安全,这虽然给企业及行业规范标准,但多项规范并未给出部署方案参考,如何在成本可控的范围内,部署适合企业运营模式且符合规范的数据灾备方案,这是很多制药企业面临的难题。
监管规范指导数据管理,企业面临灾备挑战
2011 年,发布《药品生产质量管理规范(2010 年修订)》(GMP),第一百六十三条:用电子方法保存的批记录,应当采用磁带、缩微胶卷、纸质副本或其他方法进行备份,以确保记录的安全,且数据资料在保存期内便于查阅。
2015 年,根据《药品生产质量管理规范(2010年修订)》第三百一十条规定,发布《计算机化系统》附录,作为其配套文件。
第十九条,必须采用物理或者电子方法保证数据的安全,以防止故意或意外的损害。应当建立数据备份与恢复的操作规程,定期对数据备份,以保护存储的数据供将来调用。备份数据应当储存在另一个单独的、安全的地点,保存时间应当至少满足本规范中关于文件、记录保存时限的要求。
2020 年,发布《药品记录与数据管理要求(试行)》,以进一步规范药品研制、生产、经营和使用活动的记录与数据管理。
第二十一条,系统生成的数据应当定期备份,备份与恢复流程必须经过验证,数据的备份与删除应有相应记录。第二十六条,经计算机(化)系统采集与处理后生成的电子数据,其系统应当符合相应的规范要求,并对元数据进行保存与备份,备份及恢复流程必须经过验证。
诸多规范都提出要确保电子方法保存的数据安全,并进行有效备份,同时需确保可被恢复。
五大灾备核心,群晖备份一体机满足合规要求
还是拿制药企业举例,其数据类型根据来源和用途大致分为:基础信息、行为活动数据、计量器具数据、电子数据以及文档、影像、音频等。其特点有巨量化、非结构化或半结构化。而随着 AI 人工智能技术的加入,新药研发及临床试验数据更为繁杂且庞大。总结就是平台多、增量快、类型丰富。
不同行业对于原始数据的记录和存储管理肯定有着不同的管理规范,对于和制药行业一样,非结构化数据占多数,且数据来源多、种类丰富、增量快的行业来说,可以归纳出以下五大备份核心需求。群晖希望企业借助一体化的备份方案,不仅满足行业规范要求,更可以有效抵御潜在的内外安全事件。
完整备份:电子方法保存的质量标准、工艺规程、操作规程、记录、报告等是否可以完整备份?
定期备份:数据可否实现定期备份,以避免人为损坏或勒索病毒?
异地灾备:备份数据是否存在于不同地点和不同媒介?
备份存档:备份数据是否可实现存档,并且无法被篡改以保留原始数据?
备份验证及还原演练:备份及恢复过程是否万无一失?

企业运行过程是否合规,是关乎到可否持续运营的关键。以制药企业来说,不断发生企业不符合 GMP 规范而受到处罚的事件,不仅没收违法所得,还会并处罚款,以及停产停业整顿。
通过对不同行业的合规了解,群晖备份一体机不仅可以为关键数据和设备提供灾备保护,还能满足存档要求,实现数据不可变,有效避免内外潜在的安全隐患。
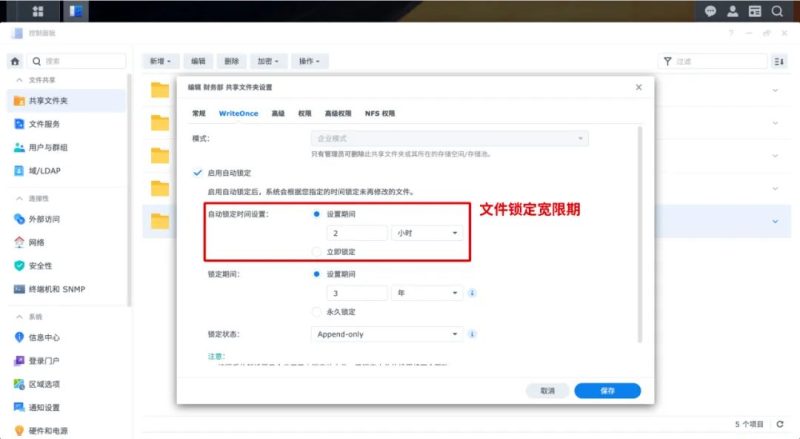
群晖 WriteOnce 实现锁定文件,无法篡改及删除文件,满足企业归档要求。
而经过多年累积,已超过一半的百强企业选择群晖,搭建灾备中心。




